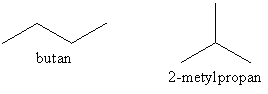Izomerizare
Izomerizarea este un proces chimic în cadrul căruia o moleculă trece în altă moleculă care are exact aceeași atomi, dar diferă prin aranjamentul atomilor în moleculă (compușii sunt izomeri).[1] Pentru unii compuși, în unele condiții specifice, reacțiile de izomerizare se produc spontan și se stabilește un echilibru chimic între formele izomere.

Exemple
La alcani
Izomerizarea are aplicații în procesele industriale de cracare, în care combustibilii precum normal-pentanul sunt încălziți în prezența unui catalizator de platină. Produșii de reacție, alcani cu catenă liniară și ramificată, se pot separa:
Un alt procedeu industrial se bazează pe izomerizarea n-butanului în prezență de clorură de aluminiu în cantități catalitice, când se obține izobutanul.
La cicloalcani
La compuși organometalici
Vezi și
- Racemizare
- Reacție de transpoziție
- Epimer
Referințe
- ^ IUPAC, Compendium of Chemical Terminology, Ed. a 2-a („Gold Book”) (1997). Versiune online: (2006-) „isomerization”.
| ||||||||||||||||||||